Vos questions
On a tous vu ces affirmations sur les réseaux sociaux, pourtant il n’y a AUCUNE donnée clinique (étude sur l’humain) ou préclinique (étude sur l'animal) qui indiquerait un effet - bénéfique ou délétère - sur la fertilité ou la reproduction. Si l’on remonte à la source de cette désinformation, elle pourrait être issue des critères d’exclusion de l'essai de Phase III des vaccins, dont ceux basés sur l'ARNm. Les femmes enceintes en étaient initialement exclues et les femmes prenant part à l'étude devaient avoir un système de contraception. Ces précautions initiales pourraient être à l’origine de cette désinformation.
Quatre vaccins contre la Covid-19 sont aujourd'hui disponibles en France :
- Le vaccin Pfizer/BioNtech sous le nom de Comirnaty® (vaccin à ARNm)
- Le vaccin Moderna sous le nom de Spikevax® (vaccin à ARNm)
- Le vaccin AstraZeneca sous le nom de Vaxzevria® (vaccin à vecteur adénovirus)
- Le COVID-19 Vaccine Janssen® (vaccin à vecteur adénovirus)
La vaccination post infection est maintenant ouverte dès le deuxième mois avec une dose de vaccin ARNm (Pfizer ou Moderna). L'infection COVID doit être confirmée par un test PCR positif (au moment de l’infection) ou par un test sérologique (après l’infection) confirmant l'infection par le virus du SARS-CoV-2.
Rapprochez-vous d'un centre de vaccination pour prendre un rendez-vous dès le deuxième mois après les résultats confirmant l'infection, pour une injection unique qui finalisera votre protocole vaccinal.
Texte de référence :
https://solidarites-sante.gouv.fr/IMG/pdf/dgs-urgent_61_precisions_campagne_vaccinale.pdf
On entend beaucoup de rumeurs à ce sujet : “on n'a pas de recul sur les vaccins à ARNm”, “ils n'ont pas été testés suffisamment longtemps”. Ceci est faux : les vaccins ARNm sont le résultat de décennies de recherche et d'essais.
Les vaccin ARNm sont en développement depuis plus de vingt ans et les études incluent la stabilité de l'ARNm mais également le moyen d'amener l'ARNm dans les cellules, les lipides. Les nanoparticules de lipides qui contiennent les ARNm et les protègent ont même été étudiées pour favoriser leur capture par les cellules dendritiques, un type cellulaire qui est une des pierres angulaires pour développer une réponse immunitaire adaptative. Donc même dans le choix des lipides il y a eu des années de recherches.
Autre point à comprendre : avant de faire des études chez l'humain, la toxicité des composants et du produit fini sont testés chez les animaux, et ce n'est que lorsque tous les feux sont au vert que l'on commence la Phase I.
Avant la COVID, BioNTech était connu en oncologie pour son approche vaccinale. Chez les patientes et patients atteints de cancer, leur objectif était d'initier une réponse immunitaire contre les cellules tumorales en développant une immunité cellulaire en plus de l'immunité humorale. En d’autres termes, l'objectif est d'aider la patiente ou le patient à combattre la tumeur grâce à son propre système immunitaire, en l'entraînant à reconnaître les cellules tumorales.
Une de leurs premières publications dans le domaine date de 2003 (https://pubmed.ncbi.nlm.nih.gov/21045153/), elle décrit des travaux conduits dans les mois et années qui précèdent la publication. Si l’on regarde le pipeline des différents projets de BioNTech, on observe qu'avant la COVID, BioNTech avait déjà une grande diversité de projets, certains en Phase I et Phase II, donc avec des composants lipides et ARNm, dont les effets indésirables avaient DÉJÀ été étudiés:
- 15 projets précliniques
- 11 projets Phase I
- 1 projet Phase II (contre mélanome)
- 1 projet Phase III (SARS-COV-2)
C'est faux.
- Le test PCR détecte la présence du génome du virus
- Le test antigénique ou TAG détecte la présence de la protéine de la nucléocapside du virus
- Le vaccin vous permet de développer des anticorps contre la protéine Spike.
Oui. La réponse immunitaire est basée sur les anticorps et les lymphocytes T. Ces deux parties de la réponse immunitaire sont induites par tous les vaccins autorisés en Europe. Les informations relatives à l'échappement immunitaire de certains variants sont issues d'expériences in vitro qui démontrent que certains anticorps (sur la panoplie de tous ceux induits par la vaccination) perdent de leur efficacité. Cependant, comme la réponse humorale (anticorps) est polyclonale, c'est-à-dire dirigée contre une multitude de fragments de la protéine Spike, seuls ceux touchés par les mutations présentes dans les variants perdent de leur efficacité. Ce n'est donc qu'une portion de la réponse. Par ailleurs, cette perte d’efficacité correspond uniquement à la réponse humorale, car la réponse cellulaire des lymphocytes T n'est pas facilement évaluée en laboratoires de ville.
Des publications récentes confirment l'efficacité des vaccins contre les variants sur la base d'essais in vitro et les données en vie réelle en Israël et au Royaume-Uni le confirment.
Les données indiquent également qu’il faut les deux doses pour être pleinement protégé, la première dose n’apportant qu’une protection partielle de 30%.
https://www.nature.com/articles/s41586-021-03777-9
Lors des études cliniques de Phase III pour les vaccins ARNm, Pfizer/BioNTech et Moderna avaient défini une limite d'inclusion de 42 jours (6 semaines) comme intervalle maximal entre les deux doses. Pour le vaccin Pfizer/BioNTech, la seconde dose doit être administrée dans les 3 à 6 semaines suivant la première dose, et pour Moderna entre 4 et 6 semaines.
Cet intervalle n'est pas choisi au hasard, il correspond aux données d'optimisation pré-clinique (chez l’animal), mais également à la réponse immunitaire. Après l'injection d'un antigène, le système immunitaire déclenche une réponse qui culmine aux environs de 14 jours, puis l'antigène ayant été éliminé, la réponse immunitaire commence à régresser (contraction immunitaire).
L'intérêt du rappel après 3-6 semaines est de réactiver cette réponse afin de l'amplifier tant au niveau des anticorps que des lymphocytes spécifiques de l'antigène, et ainsi permettre une protection optimale et la pérennité de la mémoire immunitaire.
La mortalité de la COVID est variable en fonction de l'âge mais également en fonction des comorbidités. Ces dernières, comme l'obésité, peuvent augmenter le risque d'une personne de 50 ans de faire une forme grave, par rapport aux individus de sa classe d'âge ou même à des individus plus âgés sans comorbidité. Le risque est plus important pour les hommes que pour les femmes.
Les jeunes de 0-20 ans sont très peu à risque de formes graves ou de décès, on constate cependant des hospitalisations pour des individus ayant des facteurs de risque. Le risque de décès est donc pour cette classe d'âge 1/100 000 voire moins. En dessous de 20 ans, elle est estimée à moins de 1 mort sur 1 million. Entre 20 et 40 ans, la mortalité varie entre 1 sur 10 000 et 1 sur 1000, ce qui n’est pas négligeable.
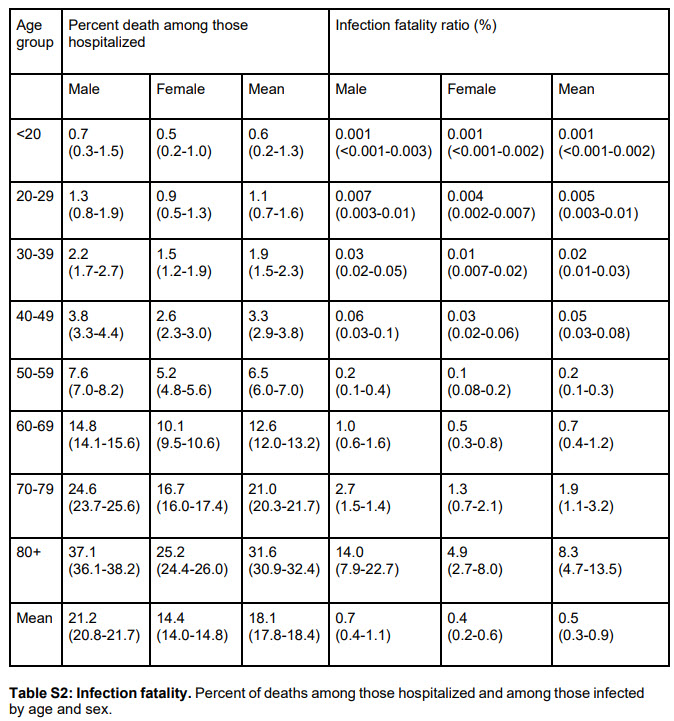 Au-delà de ces pourcentages qui ne tiennent pas compte des facteurs individuels aggravant, il ne faut surtout pas oublier que considérer le critère décès seul est très réductionniste. Etre infectée c'est prendre un risque beaucoup plus élevé de terminer a l'hôpital ou en réa et de devoir vivre des suites de l'hospitalisation et des symptômes de COVID long.
On estime aujourd'hui que 30% des personnes hospitalisées (soit environ 8% des cas COVID totaux) auront des symptômes sur plusieurs semaines et mois. Les exemples de trentenaires qui n'arrivent plus a monter les escaliers sans etre essoufflés, ou tellement fatigués que reprendre une vie socio-économique est quasi-impossible. Et cela touche toute les classe d'âge avec un pourcentage bien plus élevé que les décès.
Au-delà de ces pourcentages qui ne tiennent pas compte des facteurs individuels aggravant, il ne faut surtout pas oublier que considérer le critère décès seul est très réductionniste. Etre infectée c'est prendre un risque beaucoup plus élevé de terminer a l'hôpital ou en réa et de devoir vivre des suites de l'hospitalisation et des symptômes de COVID long.
On estime aujourd'hui que 30% des personnes hospitalisées (soit environ 8% des cas COVID totaux) auront des symptômes sur plusieurs semaines et mois. Les exemples de trentenaires qui n'arrivent plus a monter les escaliers sans etre essoufflés, ou tellement fatigués que reprendre une vie socio-économique est quasi-impossible. Et cela touche toute les classe d'âge avec un pourcentage bien plus élevé que les décès.
 Les symptômes de COVID long sont encore aujourd'hui complexe, et font débats sur leur classification (perte de goût et d’odorat, fatigue chronique, problèmes cardiaques et respiratoires), et vous pouvez retrouver un article a ce sujet sur notre site: https://ducotedelascience.com/symptomes-post-covid-un-etat-des-connaissances/). Il faut également bien garder a l'esprit que la prise en charge des ces personnes atteintes de COVID long est active, mais demandera du temps et handicapera les patients souvent pendant de longues semaines ou mois
Les symptômes de COVID long sont encore aujourd'hui complexe, et font débats sur leur classification (perte de goût et d’odorat, fatigue chronique, problèmes cardiaques et respiratoires), et vous pouvez retrouver un article a ce sujet sur notre site: https://ducotedelascience.com/symptomes-post-covid-un-etat-des-connaissances/). Il faut également bien garder a l'esprit que la prise en charge des ces personnes atteintes de COVID long est active, mais demandera du temps et handicapera les patients souvent pendant de longues semaines ou mois
 Au-delà de ces pourcentages qui ne tiennent pas compte des facteurs individuels aggravant, il ne faut surtout pas oublier que considérer le critère décès seul est très réductionniste. Etre infectée c'est prendre un risque beaucoup plus élevé de terminer a l'hôpital ou en réa et de devoir vivre des suites de l'hospitalisation et des symptômes de COVID long.
On estime aujourd'hui que 30% des personnes hospitalisées (soit environ 8% des cas COVID totaux) auront des symptômes sur plusieurs semaines et mois. Les exemples de trentenaires qui n'arrivent plus a monter les escaliers sans etre essoufflés, ou tellement fatigués que reprendre une vie socio-économique est quasi-impossible. Et cela touche toute les classe d'âge avec un pourcentage bien plus élevé que les décès.
Au-delà de ces pourcentages qui ne tiennent pas compte des facteurs individuels aggravant, il ne faut surtout pas oublier que considérer le critère décès seul est très réductionniste. Etre infectée c'est prendre un risque beaucoup plus élevé de terminer a l'hôpital ou en réa et de devoir vivre des suites de l'hospitalisation et des symptômes de COVID long.
On estime aujourd'hui que 30% des personnes hospitalisées (soit environ 8% des cas COVID totaux) auront des symptômes sur plusieurs semaines et mois. Les exemples de trentenaires qui n'arrivent plus a monter les escaliers sans etre essoufflés, ou tellement fatigués que reprendre une vie socio-économique est quasi-impossible. Et cela touche toute les classe d'âge avec un pourcentage bien plus élevé que les décès.
 Les symptômes de COVID long sont encore aujourd'hui complexe, et font débats sur leur classification (perte de goût et d’odorat, fatigue chronique, problèmes cardiaques et respiratoires), et vous pouvez retrouver un article a ce sujet sur notre site: https://ducotedelascience.com/symptomes-post-covid-un-etat-des-connaissances/). Il faut également bien garder a l'esprit que la prise en charge des ces personnes atteintes de COVID long est active, mais demandera du temps et handicapera les patients souvent pendant de longues semaines ou mois
Les symptômes de COVID long sont encore aujourd'hui complexe, et font débats sur leur classification (perte de goût et d’odorat, fatigue chronique, problèmes cardiaques et respiratoires), et vous pouvez retrouver un article a ce sujet sur notre site: https://ducotedelascience.com/symptomes-post-covid-un-etat-des-connaissances/). Il faut également bien garder a l'esprit que la prise en charge des ces personnes atteintes de COVID long est active, mais demandera du temps et handicapera les patients souvent pendant de longues semaines ou mois
Les effets indésirables sont variables dans leur fréquence et leur intensité et d'un individu à l'autre. Ce n'est donc pas parce qu'une personne de votre entourage, sœur, cousine ou collègue de travail a ressenti une douleur à l'épaule, un fatigue passagère, des maux de tête ou une fièvre légère pour une période de 24-48 heures, que cela vous arrivera forcément à vous. Ces effets restent par ailleurs très modestes au regard des symptômes et conséquences chroniques d'une infection par le virus.
Non. Les effets indésirables sont variables dans leur fréquence et leur intensité et d'un individu à l'autre. Ils ne sont pas la traduction de la réponse immunitaire.
La présence d'effets indésirables traduit une réponse de votre corps, mais ne traduit pas la qualité ni l'amplitude de la réponse immunitaire. Encore une fois les vaccins offrent une protection proche de 90% contre les formes graves de COVID-19.
Il faudra attendre un peu pour avoir assez de recul et pour que des études dédiées soient menées sur une période de 6 mois. Il faut en effet comparer la survenue de cas de COVID longs dans une population vaccinée versus une population non vaccinée de taille et groupes d'âges similaires.
Ce que l'on peut dire cependant :
- Les cas de COVID long touchent en particulier, avec une plus haute fréquence, les personnes ayant fait une forme sévère/hospitalière de la COVID (30%+). Ces formes pour lesquelles les vaccins protègent efficacement à 90%+
- Les cas de COVID long touchent indépendamment de l'âge une proportion bien plus petite pour les personnes faisant des formes légères/modérées (5-10%), pour lesquelles les vaccins offrent également une efficacité contre les formes symptomatiques (~ 60% vis-à-vis du variant Delta).
Lorsque l’on commence un essai clinique, on définit par avance ce qui va être fait : la période, l’objectif et les critères. Pour les vaccins ARNm (Pfizer et Moderna), l'efficacité et l'innocuité ont été étudiées sur plus de 15 000 personnes en 2020. Dans ces études de Phase III, les concepteurs ont donc défini une période plutôt longue pour étudier l'efficacité : la capacité du vaccin à protéger les personnes d'une forme symptomatique ou grave (nécessitant hospitalisation) de la COVID.
La confirmation de l'efficacité a été obtenue rapidement car le virus circulant beaucoup, les risques d'infection dans le groupe contrôle et dans le groupe vacciné étaient élevés.
Cette période longue de l'étude Phase III va également permettre aux concepteurs de suivre l'évolution de la réponse immunitaire humorale (anticorps) et cellulaire (lymphocytes T) au cours du temps, et ainsi définir si la mémoire immunitaire perdure ou s'il faudrait prévoir un rappel. Avec une étude de suivi allant jusqu'en 2023 ils auront ainsi des données solides.
Cet argumentaire d'une étude qui serait “encore en cours” joue sur une non-connaissance du public de la manière dont les essais cliniques sont réalisés. Ainsi un amalgame est fait entre efficacité prouvée conduisant à une autorisation de mise sur le marché (AMM) conditionnelle, et la continuité de l'étude visant à comprendre la persistance de la réponse immunitaire.
Il faut également rappeler que les personnes ayant reçu un vaccin Pfizer en phase 1 et 2 sont vaccinés depuis plus d’un an. Donc nous avons du recul. La pharmacovigilance existe et est capable de voir des effets indésirables sévères post vaccination s’il y en a. Après un an (les premiers volontaires ayant reçu le vaccin au printemps 2020), nous pouvons désormais affirmer que ceux-ci sont très rares pour les vaccins ARNm.
On définit l’efficacité d’un vaccin au travers de deux critères :
- l'efficacité vis-à-vis des formes symptomatiques: le vaccin vous empêche de ressentir des symptômes, même si vous êtes exposé au virus. Grâce au vaccin, votre système immunitaire aura été entraîné à reconnaître le virus et sera ainsi en capacité de répondre très vite, sans que cela se traduise par des symptômes.
- L'efficacité vis-à-vis des formes sévères/hospitalisations/décès. Dans ce cas on évalue la protection engendrée par le vaccin pour vous protéger des formes nécessitant une hospitalisation ou engendrant un décès.
- à plus de 90 % pour Comirnaty® de Pfizer/BioNTech et Spikevax® de Moderna après deux doses ;
- à plus de 80 % pour Vaxzevria® de Astra-Zeneca avec un intervalle de plus de 12 semaines entre les deux doses ; et à plus de 90 % pour les formes sévères 28 à 34 jours après 1 dose ;
- à plus de 65 % pour Covid-19 Vaccine Janssen® après une seule dose pour les formes symptomatiques, de 75 % pour les formes sévères et de 90% pour les hospitalisations.
- de l’ordre de 80 à 90 % pour les vaccins à ARNm, après deux doses
- de l’ordre de 70 % pour Covid-19 Vaccine Janssen®.
- Pour Vaxzevria® de Astra-Zeneca les données quant à l’efficacité vaccinale contre les infections asymptomatiques sont moins robustes.
Dans l'historique de la pharmacovigilance de tous les vaccins, il n’y a pas d’effets secondaires à long terme qui n'auraient pas été identifiés après deux ou trois mois.
Si on avait dû voir des effets, nous les aurions déjà vus, et c’est ce qu’il s’est passé:
- On a vu qu’AstraZeneca présentait un problème de thrombose avec un risque de 1/100.000. C’est pour ça qu’on a réservé ce vaccin aux plus âgés. Mais c’est un phénomène rare. Il y a cinq fois plus de chance d’avoir un accident de voiture qu’une thrombose. le problème a été identifié rapidement en Europe grâce à la pharmacovigilance à partir du moment où on a commencé à utiliser le vaccin AZ.
- De la même manière on a vu la petite hausse de myocardites chez les jeunes garçons de 12 à 15 ans vaccinés avec le vaccin Pfizer.
Il n’y a pas à ce jour de contre-indication à la vaccination pour les femmes allaitantes. L’OMS recommande la vaccination aux femmes allaitantes au même titre que les autres adultes.
il existe une page dédiée à cette question qui est régulièrement mise a jour:
https://info-allaitement.org/ressources-en-ligne/vaccination-covid-19-et-allaitement/
Les patients atteints ou en traitement pour un cancer sont souvent des patients à risque et qui doivent être suivis et vaccinés le plus tôt et rapidement possible. Pour certains en fonction de leurs traitements immunomodulateurs (en particulier pour les lymphopathies malignes) une troisième dose leur est administrée afin de combler leur immunité affectée par les traitements.
Les vaccins anti-COVID initient une réponse immunitaire a la fois ciblée contre Spike et également systémique/globale du fait des cytokines produite pour mobiliser le système immun. De ce fait, la vaccination induit une remontée du seuil de la surveillance immunitaire.
Cela peut avoir un effet chez les personnes qui sont traites pour leurs maladies chroniques inflammatoires (Crohn, SPA, MICI, etc.) et donc induire une réapparition partielle et temporaire des symptômes pour lesquels ils prennent des traitements immunomodulateurs.
Certains cas de régressions spontanées de cancers après une vaccination ont été décrits: Primary cutaneous anaplastic large cell lymphoma with marked spontaneous regression of organ manifestation after SARS-CoV-2 vaccination
Les vaccins a ARNm sont composés d'ARNm de Spike encapsulés dans des nanoparticules de lipides de 80nm (1 000 fois plus petit qu'un cheveu). Ces nanoparticules sont donc des lipides, et on aurait également pu utiliser le terme de "liposomes".
Le vaccin Pfizer-BioNTech - COMIRNATY dont l’ingrédient actif est constitué de l’ARNm modifié permettant de coder pour la protéine S du SARS-CoV-2, est associé à des lipides, du sucrose, du potassium, du sodium.
1. Antigène
ARNm COVID-19 (incorporé dans des nanoparticules lipidiques) : 30 microgrammes.
Il s'agit de molécules d'acide ribonucléique (ARN) messager (ARNm) simple brin, avec addition d'une coiffe en 5', produit à l'aide d'une transcription in vitro sans cellule à partir des matrices d'ADN correspondantes, qui codent la protéine virale de spicule (appelée protéine Spike ou protéine S) du coronavirus SARS-CoV-2 responsable de la COVID19.
2. Excipients
- Lipides
- (4-hydroxybutyl)azanediyl)bis(hexane-6,1-diyl)bis (ALC-3015)
- (2- hexyldecanoate),2-[(polyethylene glycol)-2000]-N,N-ditetradecylacetamide (ALC0159)
- 1,2-distearoyl-snglycero-3-phosphocholine (DPSC)
- cholesterol
- chlorure de potassium,
- phosphate monopotassique,
- chlorure de sodium,
- phosphate disodique dihydraté,
- saccharose,
Le vaccin Moderna SPIKEVAX , la composition d’une dose (0,5 mL) contient :
1. Antigène
100 microgrammes d'ARN messager (ARNm) encapsulé dans les nanoparticules lipidiques SM-102
ARN messager (ARNm) monocaténaire, avec addition d'une coiffe en 5', produit par transcription in vitro sans cellule à partir des matrices d'ADN correspondantes, codant la protéine de spicule (protéine spike ou protéine S) du coronavirus SARS-CoV-2.
2. Excipients
- Lipides
- SM-102
- Cholestérol
- 1,2-distéaroyl-sn-glycéro-3-phosphocholine (DSPC)
- 1,2-dimyristoyl-rac-glycéro-3-méthoxypolyéthylène glycol-2000 (PEG 2000 DMG)
- Trométhamine : 0,31 mg
- Chlorhydrate de trométhamine : 1,18 mg
- Acide acétique : 0,043 mg
- Acétate de sodium trihydraté : 0,12 mg
- Saccharose : 43,5 mg
Pour références complémentaires et autres sites d’information:
- https://www.santepubliquefrance.fr/dossiers/coronavirus-covid-19/vaccination-contre-la-covid-19
- https://vaccination-info-service.fr/
- https://covaxinfo.fr/
- https://www.acsh.org/news/2020/11/18/covid-infection-fatality-rates-sex-and-age-15163
- https://ourworldindata.org/coronavirus
- https://covid19.who.int/
- Pfizer/BioNTech [BNT162b2] : Stratégie de vaccination contre le SARS-CoV-2 – Place du vaccin à ARNm COMIRNATY® (BNT162b2)
- Moderna [mRNA-1273] : Stratégie de vaccination contre la Covid-19 – Place du Vaccin Moderna Covid-19 mRNA (nucleoside modified)
- AstraZeneca [AZD1222] : Stratégie de vaccination contre la Covid-19 – Place du Covid-19 Vaccine AstraZeneca
- Janssen [Ad26.COV2.S] : Stratégie de vaccination contre la Covid-19 – Place du vaccin Covid-19 Janssen
- Stratégie de vaccination contre le Sars-Cov-2 – Actualisation des facteurs de risque de formes graves de la Covid-19 et des recommandations sur la stratégie de priorisation des populations à vacciner
- https://ansm.sante.fr/actualites/?filter%5Bcategories%5D=22
- https://ansm.sante.fr/actualites/point-de-situation-sur-la-surveillance-des-vaccins-contre-la-covid-19-periode-du-11-06-2021-au-24-06-2021
- https://www.infectiologie.com/UserFiles/File/groupe-prevention/covid-19/vaccins-covid-19-questions-et-reponses-spilf.pdf
- https://www.infovac.fr/?view=article&id=847&catid=45
- https://info-allaitement.org/ressources-en-ligne/vaccination-covid-19-et-allaitement/